Abordagem inicial da lesão tumoral
Tumores músculo-esqueléticos primários são raros. Porém, a sobrevida do paciente depende grandemente ao estágio que a doença é descoberta. Uma descoberta precoce pode ser a linha divisória entre a vida e a morte e entre a amputação e a preservação do membro. Assim, uma lesão tumoral deve sempre estar entre as suspeitas diagnósticas.
– Maioria entre 5-25 anos
– < 3% das neoplasias
– Neoplasias osseas primárias: entre as 5 mais comuns entre 10-15 anos
Os tumores ortopédicos aparecem sintomaticamente como uma ou mais destas apresentações clínicas: dor, edema, achado ocasional em exames de imagem ou fratura patológica. Cada ponto deve ser minimamente avaliado.
Dor
Geralmente apresentam dor.
A dor deve ser avaliada quanto ao seu caráter:
– mecânica (piora com movimento)
– contínua
– pior durante a noite
– período de tempo.
– Pode ter relação com atividade
– Geralmente dão dor progressiva, ao repouso e à noite
– Alguns tumores benignos, principalmente o osteoma osteóide
– Tumor de partes moles geralmente não apresentam dor, com exceção dos tumores de bainha nervosa
Edema
Quanto ao edema ou à tumoração evidente deve-se questionar o período de aparecimento e associação com trauma local, além de avaliar a consistência da massa: pétrea, fibrosa, etc.
Exame físico
O exame físico é muito importante para avaliar-se o tamanho da lesão, a consistência, como já dito e as possíveis alterações tanto neurológicas quanto sistêmicas.
– Manchas café-com-leite ou hemangiomas
– Linfadenomegalia: metástase para linfonodo é rara na maioria dos sarcomas
– Metástase geralmente freqüente em rabdomiossarcoma, sarcoma epitelióide e sarcoma sinovial
Observação criteriosa também deve ser feita quanto a idade, sexo e raça do paciente, pois alguns tumores ocorrem em certas épocas da vida, alguns são raros em negros e amarelos e outros possuem diferenças quanto ao sexo.
– Sexo: alguns tem predileção por sexo (TGC: sexo feminino) mas não há relevância para diagnóstico
– Raça é pouco relevante: sarcoma de Ewing é muito raro em negros
– História familiar é útil em várias doenças: exostose hereditária múltipla; neurofibromatose
– Idade: muito importante
Laboratório
Testes laboratoriais são usados, sendo muitos contribuintes para ajudar no diagnóstico:
– fosfatase alcalina (osteossarcoma)
– – Fosfatase alcalina: 50% dos osteossarcomas. Se muito alta: pensar em multicêntrico
– desidrogenase lática (PNET)
– VHS e PCR (infecções)
– VHS aumenta:
– – Ewing (pior prognóstico), linfoma ósseo, leucemias, tumores metastáticos, OMC, histiocitose
– PSA (metástases de carcinoma de próstata), etc.
Exames de imagem
Nos exames de imagem a radiografia simples deve ser o marco inicial e muitas vezes é o exame que mais nos dá informações. Devemos nos lembrar das perguntas de Enneking:
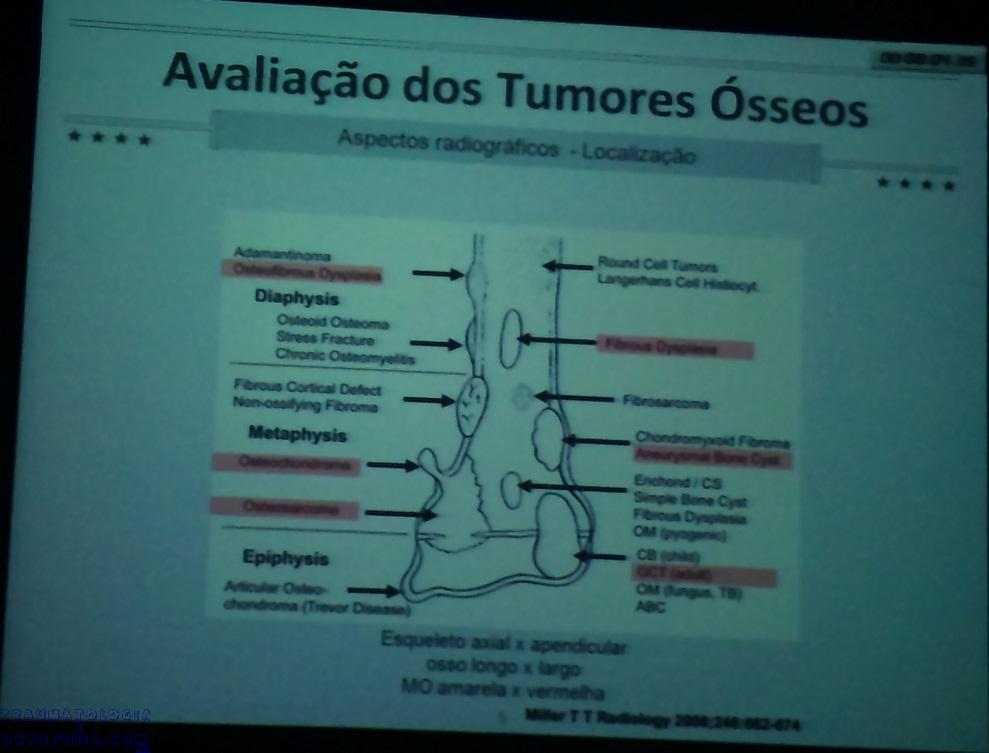
– “Onde está a lesão no osso?” (epífise, metáfise ou diáfise)
– “O que a lesão faz com o osso?”
– “Como o osso normal responde à lesão?”
– “Algo sugere algum tipo histológico específico?”.
RX: todos devem ser investigados por RX simples
– Corpo vertebral em crianças: geralmente granuloma eosinofílico
– Elementos posteriores das vértebras: osteoblastomas ou cisto ósseo aneurismático
– Pelve: Ewing na infância e Ewing ou condrossarcoma no adulto
– Costelas: displasia fibrosa ou Ewing
– Epífise com fise aberta: condroblastoma epifisário.
– Outros: granuloma eosinofílico ou osteomielite
– Epífise com fise fechada: TGC (se placa aberta, TGC pode acometer a metáfise)
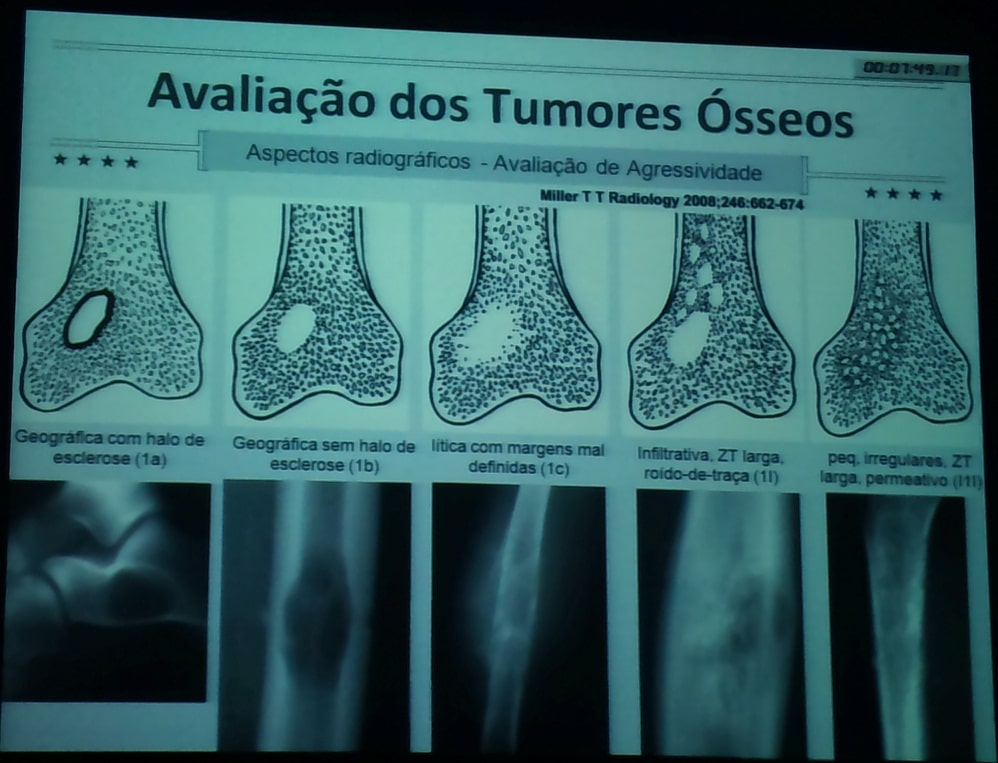
– Inativa: borda bem definida com formação de osso reativo na borda
– Agressiva: borda mal definida de transição entre a lesão e osso
– Expansão cortical pode ser vista com doença benigna agressiva mas destruição intensa da cortical é sinal de malignidade
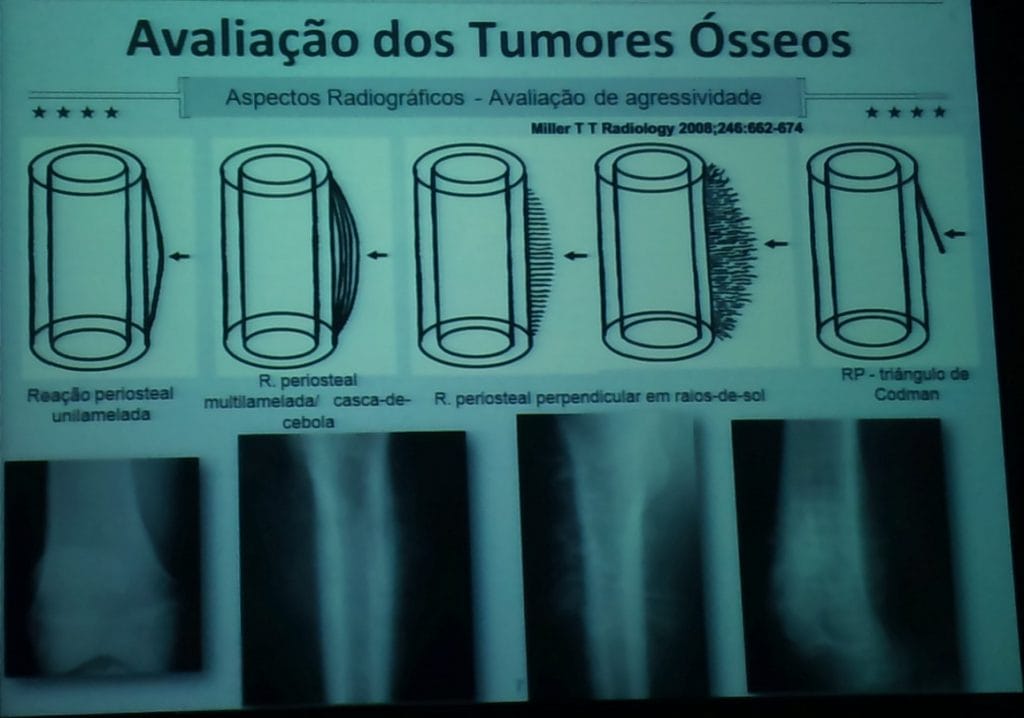
– Reação periostal com formação de osso novo ocorre quando há destruição cortical
– Padrões:
– – Triângulo de Codman
– – Casca de cebola
– – Raios de Sol
– Geralmente sinal de malignidade, mas pode ocorrer com infecção ou histiocitose
– Ossificação: mineralização de matriz óssea
– Calcificação: mineralização sem estrutura, aparece desordenada e mais densa do que ossificação -> Tumores cartilaginosos
– RX tem menor importância em lesões de partes moles
– – Flebolito no hemangioma
– – Calcificação no sarcoma sinovial
– – Densidade de gordura no lipoma
– – Presença de miosite ossificante
Nos achados ocasionais em exames de imagem deve-se verificar por que o exame foi pedido e sintomas prévios ao exame.
A fratura patológica é um evento que envolve dor e preocupação de pais. Avaliar sintomas prévios, mecanismo de fratura e características da mesma.
A tomografia computadorizada é um bom método para a avaliação do comprometimento cortical e de outros detalhes ósseos. Auxilia também na avaliação da ossificação e da calcificação da matriz. É o exame padrão ouro para avaliar a presença de metástases pulmonares.
– Bom para definir área da lesão
– Foi em parte substituída pela RM
– Mais útil para avaliação da ossificação e calcificação e integridade cortica
A ressonância magnética é o melhor método para avaliar a extensão intra e extramedular do um tumor ósseo. Ótimo exame para avaliar as partes moles.
– Boa para delimitar as massas
– Limitada para diferenciar lesões malignas de benignas
– Lesões > 5 cm ou profunda à fáscia: aumento do risco de ser sarcoma
A cintilografia óssea é um bom método para avaliar também de certa forma o tamanho e extensão do tumor, mas principalmente para verificar a presença de metástases, como as metástases saltitantes.
– Aumento de captação
– aumento do fluxo sanguíneo
– Mineralização ativa: persiste após 3 horas.
– Atividade do Tc99m acaba com 6 horas
– Indicado para pesquisa de metástases e determinar a localização de lesões múltiplas em osteocondroma, encondroma, displasia fibrosa e histiocitose
– Frequentemente é falso negativa no mieloma múltiplo
– Podem ser frias também no granuloma eosinofílico e sarcoma intensamente anaplásico
– Com exceção do mieloma, todas as neoplasias ósseas malignas aparecem com aumento na captação à cintilografia com Tc99m
– Exame negativo tranqüiliza, mas exame positivo não demonstra se lesão é maligna ou benigna
Outros exames como a arteriografia e a ultra-sonografia são menos usados, mas podem ter espaço no estadiamento das lesões. A arteriografia pode avaliar a condição dos plexos vasculares e ser útil também para avaliar a resposta do tumor á quimioterapia (diminuição da vascularidade).
Biópsia
Só após uma perfeita investigação e um bom estadiamento, com algumas hipóteses diagnósticas deve-se pensar ou não em biópsia. Esta deve, de preferência, ser feita por profissional especialista em oncologia ortopédica e pelo profissional que irá dar seguimento ao tratamento do paciente.
– Se usar garrote, fazer por elevação
– Incisão longitudinal
– – Fazer através de um compartimento muscular e não através do plano intermuscular
– – Evitar estruturas neurovasculares
– Se for necessário fazer orifício ósseo, fazê-lo oval ou redondo
– Fechar o buraco com metacrilato para limitar a formação de hematoma
– – Fechamento do orifício: menor disseminação local e maior disseminação sistêmica
– Retirar a periferia da lesão: maior quantidade de tecido viável
– Área do triângulo de Codman não ajuda no diagnóstico
– Neoformação óssea periosteal reacional pode ser interpretada como área formadora do tumor
– Se usar dreno, colocá-lo pela incisão
– Ressecção primária só deve ser feita se: massa subcutânea < 5 cm, provalvemente não é maligna
– – 1/3 dos sarcomas de partes moles é subcutâneo e com frequência têm < 5 cm
– Técnicas de biópsia
– – Incisional: ressecção direta de uma amostra de tecido
– – Excisional: é uma ressecção marginal
Descrição Radiológica dos Tumores
1 – Lesão:
Solitária;
Múltipla ou disseminada;
2 – Qual osso comprometido;
3 – Segmento ósseo:
– Epífise;
– Metáfise;
– Diáfise;
4 – Local no osso:
Central;
Excêntrica;
Cortical;
Subperiosteal;
5 – Reação do osso à lesão:
Rarefação (lise);
Condesação (esclerose);
Rarefação/condensação;
6 – Limites da lesão:
Precisos;
Imprecisos;
7 – Comprometimento Cortical:
Insuflada -> remodelação;
Periosteal -> interrompida;
8 – Reação Periosteal:
Ausente / presente;
Lamelar -> sólida / espicular -> fina;
9 – Massa tumoral extra-cortical: Ausente; Presente.
Chegou com você no Pronto Socorro
Iniciar sempre com Rx. Primeiro avaliação total com outras provas, depois biópsia.
– hemograma: infecção e leucemia
– VHS: infecção, carcinoma metastático, sarcoma de Ewing, linfoma, leucemia e histiocitose
– PSA: próstata
– Hipercalcemia: doença metastática, mieloma múltiplo, hiperparatireoidismo (TSH/PTH)
– FAL: doença óssea metabólica, osteossarcoma, sarcoma de Ewing ou linfoma. Se ligações cruzadas urinárias de piridínio = Paget
– Uréia e creatinia: tumores renais + hematúria no EAS
– Enzimas hepáticas e eletrólitos para metastáses desconhecidas
– Qualquer tecido mole profundo à fascia ou com mais de 5 cm na sua maior dimensão = maior probabilidade de sarcoma
TC: avaliar metástases. Ossificação, calcificação e integridade da cortical, ex: osteoma osteóide, metástases pulmonares pequenas
Cintilografia: implantes no corpo. Negativo: exclui -> exceção é o mieloma múltiplo; Positivo: não diferencia benignos de malignos
RM: definir extensão de alguns diagnósticos prováveis. Não diferencia benignos de malignos.
Imuno-histoquímica:

| Tipo | Histologia | Características | Clínica | D Diferencial | Tratamento |
| Osteoma Crianças e adolescentes | Tecido osteoblástico, osso maduro, bem diferenciado. Crescimento lento | Adensamento homogêneo. Crânio, face, seios paranasais – frontal e etmoidal (75%), mandíbula | Freqüência baixa | Osteossarcoma justacortical (quando aparece em ossos longos) | Lesões benignas latentes. Acompanhar clinicamente. Cirurgia se comprimir estruturas. Malignização não é relatada. |
| Osteoma Ostóide Adolescentes e adultos jovens | Osteoblástico. Nicho com osteóide (osso imaturo) | < 1,5 cm, com bordos definidos e zona de reação periférica periosteal (não constante) Ossos longos (65%), diáfise da tíbia e do fêmur, tb nas vértebras (arco neural). | Lesão dolorosa, persistente, piora à noite e melhora com AINE (pp salicitatos) Não costuma haver aumento de volume. Ocorre mais na cortical. RNM não é válida | Osteoblastoma (pq é menor, maior grau de esclerose circundante e menos agressivo) | Bom prognóstico com a evolução natural ou cirurgia Ressecção ampla do nicho e área de esclerose ao redor Procedimentos intracapsulares não devem ser feitos |
| Osteoblastoma Infância e adolescência | Semelhante ao osteoma osteóide | >1,5 cm, sem esclerose circundante, maior agressividade Vertebras (50%), ilíaco, costelas e ossos das mãos e dos pés | Menos doloroso que o osteoma osteóide Lesões osteolíticas (rr osteoblásticas), área central pode ser transparente, mas, em geral, tem maior densidade. Pp intramedular | Em geral bem circunscritos, mas destruição pode se mostrar agressiva podendo sugerir lesão maligna | Ressecção com margens amplas com bom prognóstico |
| Condroma | Cartilagem madura. Frequentes. Encondromatose múltipla unilateral -> Ollier => associada com hemangioma -> Maffucci | Lesões líticas. Ossos das mãos e dos pés, nas costelas e ossos longos. | Em geral no centro, encondroma. Imagem ovóide, que afila e insufla a cortical adjacente. Aspecto algodonoso da matriz. | Condrossarcoma, as vezes, difícil Na idade adulta pode desenvolver maliginidade -> acompanhar com TC | Marginal, com curetagem e enxertia. Malignização (invade cortical) rara na encondromatose solitária de mãos e pés. |
| Condroblastoma Entre 10 e 17 anos. Fise aberta | Tecido celular, relativamente indiferenciado, do tipo osteoclástico. Zonas de calcificação focal. Tumor de Codman | Epifises dos ossos longos, as vezes, até a metáfise contígua. Proximal da tíbia, distal do fêmur e proximal do úmero. | Queixa articular freqüente -> derrame sinovial (invasão da articulação 10%) Área lítica, arredondada, de 1-4 cm, delimitado por osso esclerótico. Pode ter calcificação moteada e destruição do osso. | Curetagem e enxertia cuidadosa, tomando cuidado com a fise. | |
| Osteocondroma Infância e adolescência | Exostose óssea recoberta por cartilagem Tumor benigno mais comum (10%). Exostose múltipla | Ossos com ossificação endocondral -> metáfise distal do fêmur e proximal da tíbia, proximal do úmero e do fêmur. Cresce da metáfise para diáfise. | Pode formar uma bolsa devido irritação da musculatura e tendões. Pode ocorrer fratura da base da exostose. A cartilagem não é vista no Rx. | Não tem relação com malignidade Crescimento rápido e dor sugerem maliginização (0,1%) | Ressecção quando houver compressão, alterações funcionais e inflamação da bursa |
| Condroma Fibromixóide Puberdade e adolescência | Cartilagem com tecido mixóide e fibroso. Mais rara. | MMII -> tíbia (50%), fêmur, metatarso e calcâneo. Queixa clínica mínima. | Área arredondada, excêntrica, na região metafisária de ossos longos, Halo reacional. | Cisto ósseo aneurismático | Curetagem e enxertia. Cuidado com placa de crescimento. Recorrência rara. |
| Cisto unicameral Infância e adolescência, após, sacro e calcâneo | Cavidade repleta de líquido claro ou sanguinolento(trauma), revestida por membrana com osteoclastos. | Metáfise proximal do úmero e do fêmur. Dor e tumefação | Os que se afastam da placa de crescimento são latentes. Fraturas modificam o aspecto. Bem delimitado, com abaulamento. Sinal da espícula caída. Centro. | Cisto ósseo aneurismático, difere pq não tem reação periosteal, com mínima oou nenhuma expansão do osso. | MMSS conservador. MMII curetagem + enxertia |
| Cisto aneurismático Crianças, adolescentes e adultos jovens | Lesão osteolítica expansiva, cheios de sangue | Região metafisária dos ossos longos e coluna vertebral ; Excentrico, insufla a cortical e destrói a metáfise-epifíse. Dor local de várias semanas a meses | 3 estágios: 1 restrito a esponjosa; 2 excêntrico, insuflando a cortocal(bolha de sabão e casca de ovo), pode ter casca de cebola e triângulo de Codman; 3 osso destruído | Osteossarcoma telangiectásico e tumor de células gigantes | Ressecção ampla com enxertia. |
| Cisto justarticular Ganglion intraósseo Após 14 anos | Localizado no osso subcondral, junto a articulação. Tecido fibroso com áreas de tecido mucóide | Distal e proximal da tíbia. Edema, raro tumor palpável. | Osteolítica, com esclerose circundante. excentrica | Curetagem + enxertia | |
| Granuloma eosinófilo (de células de Langerhans) Histiocitose X Mais jovem, mais grave | Elementos retículo-histiocitários, solitárias ou mútiplas (síndrome de Hand-Schüller-Christian ou da Enfermidade de Letterer-Siwe) | Crânio, fêmur, mandíbula, costelas, vértebras (plana de Calvé) e ossos chatos Dor por semanas ou meses, tumefação, sinais inflamatórios, febre, VHS, leucocitose | Diáfises, osteolíticas, “casca de cebola” | Tumor Ewing e osteomielite | Cura espontânea. Sintomático: Curetagem + enxertia. Contraindica injeção de corticóides |
| Defeito fibroso cortical (fibroma não-ossificante – dor e crescimento) Crianças e adolescentes | um tecido fibroso, disposto em rodamoinhos, nos quais se podem observar numerosas células gigantes multinucleadas, pigmento de hemossiderina e histiócitos repletos de lipídios | Metáfise de ossos longos, fêmur e tíbia | pequenos defeitos líticos, claramente delimitados por halo de esclerose | Conservador. Em caso de fraturas, intralesional com enxerto | |
| Ossificação heterotrópica (miosite ossificante) | proliferação de tecido fibroso e pela neoformação de grande quantidade de osso, as vezes relacionado com traumatismo | Não envolve o córtex da lesão Dor e inchaço localizado | Somente após 4 semanas começa a aparecer -> TC | Osteossarcoma justacortical e sarcoma de partes moles | Conservador. Quando houver bloqueio pode-se pensar em ressecção. |
| Displasia fibrosa Esqueleto em desenvolvimento | tecido fibroso-conjuntivo disposto em rodamoinhos, no qual se encontram trabéculas mal orientadas de osso imaturo e não lamelar, que tendem a formar figuras em forma de “S” ou “C”. | Fêmur, tíbia, ossos da face e costelas. Dor, deformidade, distribuição segmentar | lesões radiolúcidas intramedulares, “vidro fosco”. | Encondroma, cisto ósseo unicameral, neurofibromatose | Monostóticas conservador. Poliostóticas, grande quantidade de enxerto. Quanto mais tarde melhor. |
| Tumor marrom 3ª e 4ª décadas, mulheres | áreas osteolíticas, de aspecto cístico, principalmente nos ossos longos e maxilares. pela excessiva produção de hormônio paratireoideano paratireóide | Conseqüente reabsorção osteoclástica associada à hipercalcemia e hipofosfatemia. O excesso de destruição tenta ser compensado pela neoformação óssea, resultando em aumento de fosfatase alcalina. | Lesão radiotransparente, com margens pouco definidas. | Tumor de células gigantes, porém atingem mais as diáfises | Tratar o hiperparatireoidismo Proteção contra fraturas. |
| Tumor de células gigantes 20-40 anos Placas epifisárias fechadas | Muito vascularizado, numerosas células gigantes do tipo osteoclástico (núcleos não são hipercromáticos, nem anaplásicos) | 50% ao redor do joelho, epífises de ossos longos -> distal do fêmur, proximal da tíbia e distal do rádio. Vértebra acomete o corpo. Dor e aumento de volume. Pode sinovite. | Osteolítico, destrói a epífise, insufla a cortical, invade metáfise e chegca até a cartilagem. Classificação de Campanacci em 3 graus. | Cisto ósseo aneurismático, condroblastoma Malignização para fibrohistiocitoma ou fibrossarcoma após radioterapia | Retirar todo o tumor |
– Podem confundir com osteossarcoma no exame patológico -> miosite ossificante e calo de fratura.
– Tumores malignos -> reação periosteal fina -> triângulo de Codman e raios de sol
– Tumores benignos -> reação lamelar grossa -> tem tempo para amadurecer
– Periósteo -> calo ósseo, granuloma eosinófilo e osteomielite.
> Arquivos de Apresentações em ppt
> Arquivos de Resumos em pdf